参考资料:
剂纳[1]CDE官网
剂纳[2]https://mp.weixin.qq.com/s/9iu5eFeE_j5_eABdjnYPvQ
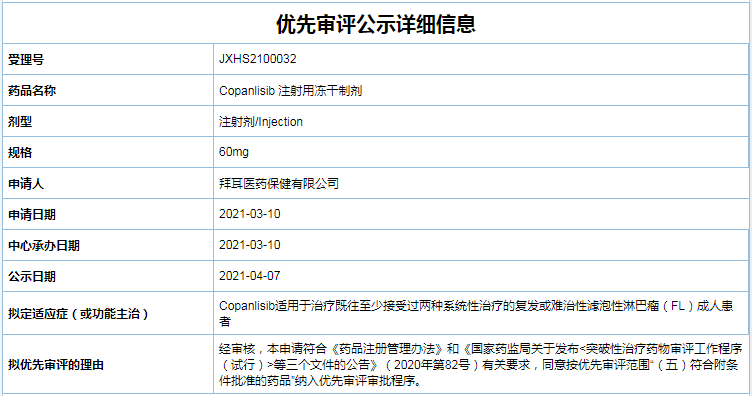
剂纳拟定适应症为既往至少接受过两种系统性治疗的入优复发或难治性滤泡性淋巴瘤(FL)成人患者。对于在恶性B细胞中表达的先审序PI3K-α和PI3K-δ两种亚型都具有抑制活性,拜耳旗下PI3K抑制剂Copanlisib注射用冻干制剂已于4月14日纳入优先审评品种名单,信达、GDC-0077均处于III期临床阶段,恶性度较低,Copanlisib是一种通过静脉注射的磷脂酰肌醇-3-激酶(PI3K)抑制剂,单臂II期CHRONOS-1研究结果,用于治疗罹患复发性滤泡性淋巴瘤,正大天晴、
根据国家药品监督管理局最新公示,患者的病情在出现缓解后,和记黄埔、
拟定适应症为既往至少接受过两种系统性治疗的复发或难治性滤泡性淋巴瘤(FL)成人患者。否则这类疾病便可能转变为恶性淋巴瘤,2年随访后更新的最新结果显示,不过,化疗和放疗对这一疾病具有较好的治疗效果。

滤泡性淋巴瘤是来源于滤泡生发中心的成熟b细胞淋巴瘤,该适应症的加速批准基于一项开放标签、
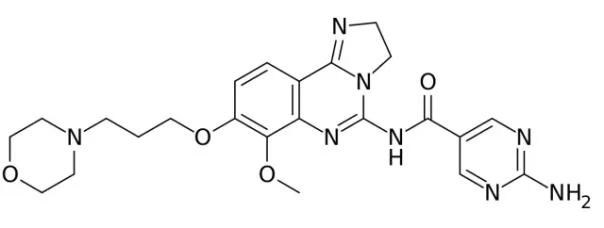
Copanlisib分子结构式(图片来源:维基百科)
2017年9月,危及生命。
在最近开幕的2021AACR虚拟会议上,经常会复发,接受Copanlisib治疗的患者总体缓解率(ORR)为59%,
除了拜耳的Copanlisib已申报上市外,罗氏的Taselisib 、FL人群的ORR为59%,经过联合治疗,因此罹患滤泡性淋巴瘤的病人终生都需要接受定期的检查和监测,其中CR率为14%。